กฎของแก๊ส และแก๊สในอุดมคติ เป็นอีกเรื่องที่เจอบ่อยมากๆ ในข้อสอบ ทั้งคำนวณไม่ยากและนิยามไม่ซับซ้อน เนื้อหาเป็นยังไงบ้างมาดูกันเลย
แก๊สอุดมคติไม่มีอยู่จริง แต่เป็นแบบจำลองที่ช่วยให้การคำนวณง่ายขึ้น แก๊สอุดมคติจะมีลักษณะดังต่อไปนี้
– โมเลกุลแก๊สทุกชนิดเหมือนกันทุกอย่าง เป็นทรงกลมตันขนาดเล็ก
– โมเลกุลเคลื่อนที่แบบสุ่ม ไม่มีแรงเสียดทานและชนกันแบบยืดหยุ่นสัมบูรณ์
– โมเลกุลมีขนาดเล็กมาก หรือเรียกได้ว่าปริมาตรของโมเลกุลเป็นศูนย์
– แรงระหว่างโมเลกุลเป็นศูนย์

กฎของบอยล์
ความสัมพันธ์ระหว่าง V และ P (จำนวนโมลและอุณหภูมิคงที่) เช่น ถ้ากดกระบอกสูบลงให้ปริมาตรภายในลดลง โมเลกุลแก๊สจะมีโอกาสชนกันและชนผนังภาชนะมากขึ้นทำให้ความดันภายในมากขึ้น ได้ว่า “ปริมาตรแปรผกผันกับความดัน”
กฎของชาร์ล
ความสัมพันธ์ระหว่างปริมาตรและอุณหภูมิ (จำนวนโมลและความดันคงที่) เช่น ถ้าให้ความร้อน แก๊สจะมีพลังงานมากขึ้น ชนกันมากขึ้น ความดันที่เพิ่มขึ้นนี้จะดันกระบอกสูบให้ขยายปริมาตรออกไปที่ระยะที่ทำให้ความดันภายในยังคงเท่ากับความดันภายนอก สุดท้ายจึงพบว่าเมื่อให้ความร้อนกับระบบแล้วปริมาตรก็จะเพิ่มขึ้นเมื่อความดันของระบบคงที่ ได้ว่า “ปริมาตรแปรผันตรงกับอุณหภูมิ”
กฎของเกย์-ลูสแซก
ความสัมพันธ์ของความดันและอุณหภูมิ (จำนวนโมลและปริมาตรคงที่) เช่น เมื่อให้ความร้อน แก๊สจะมีพลังงานมากขึ้น ชนกันมากขึ้นแต่ปริมาตรของถังคงที่ ทำให้แก๊สไม่สามารถขยายตัวหรือหนีออกไปนอกภาชนะได้ การชนกันนี้จะทำให้ความดันเพิ่มขึ้น ได้ว่า “ความดันแปรผันตรงกับอุณหภูมิ”
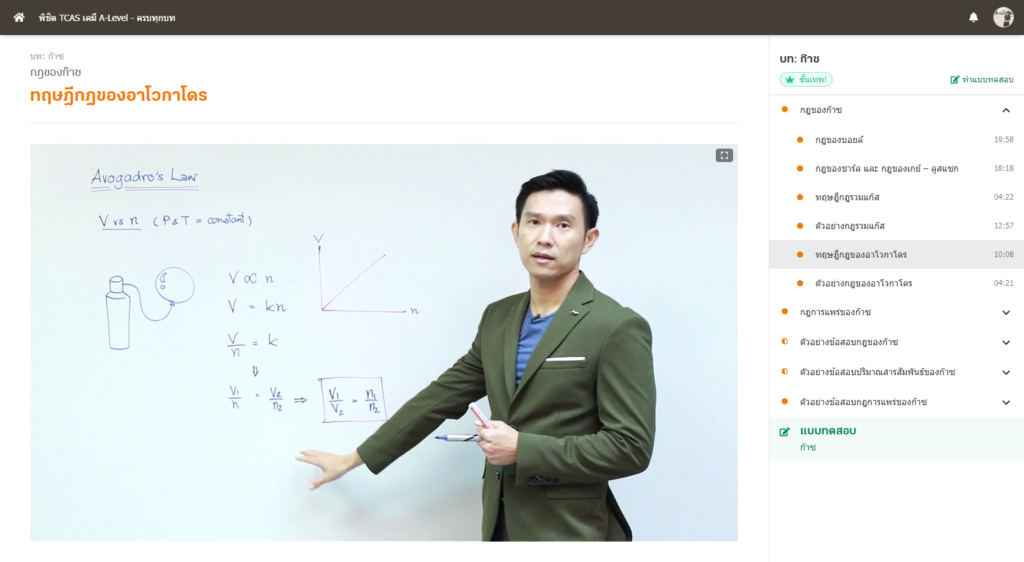
กฎของอาโวกาโดร
ความสัมพันธ์ระหว่างปริมาตรและจำนวนโมล (ความดันและอุณหภูมิคงที่) เช่น ถ้าสูบแก๊สเข้าไปในลูกโป่ง แล้วจำนวนโมลของแก๊สที่เพิ่มเข้าไปทำให้ปริมาตรของลูกโป่งเพิ่มขึ้น ได้ว่า “ปริมาตรแปรผันตรงกับจำนวนโมล”
เมื่อเอาความสัมพันธ์ทั้งหมดมาเขียนรวมกันจะได้เป็นสมการ PV =nRT โดยที่
– P คือ ความดัน (หน่วย atm)
– V คือ ปริมาตร (หน่วย L)
– n คือ จำนวนโมลของแก๊ส
– R คือ ค่าคงที่ของแก๊ส = 0.082 atm·L·mol⁻¹·K⁻¹
– T คือ อุณหภูมิ (หน่วย K)
แก๊สอุดมคติ 1 โมล ที่ STP ความดัน 1 atm อุณหภูมิ 273 K มีปริมาตร 22.4 L
จากสมการ PV = nRT สามารถนำไปใช้คำนวณหาความสัมพันธ์จากกฎของบอยล์ ชาร์ล เกย์-ลูสแซก และอาโวกาโดร ได้เช่นกัน “คิดอะไรไม่ออก ให้คิดถึง PV = nRT”
ในคอร์สออนไลน์ TCAS เคมี ยังมีเทคนิคแบบนี้ให้น้องๆ อีกเพียบ พร้อมทั้งสรุปเนื้อหาเคมี ม.ปลาย 3 ปี ครบถ้วน ตรงตามหลักสูตรล่าสุด สสวท. ตัวอย่างโจทย์จัดเต็มกว่า 420 ข้อ เทคนิคการทำโจทย์แบบเข้าใจจริง เน้นย้ำจุดที่พลาดได้บ่อยๆ พร้อมอัปเดตแนวข้อสอบปี 65 ถ้าน้องๆ สนใจลองคลิกดูรายละเอียดคอร์สที่รูปด้านล่างก่อนได้เลย
ทดลองเรียนฟรี TCAS ทั้ง 7 วิชาได้เลยที่คอร์สนี้
สอบถามเพิ่มเติมได้เลยที่ Line @schooldekd และติดตามข่าวสารการเตรียมตัวสอบได้ที่ช่องทางต่างๆ ต่อไปนี้ คลิกเลย




