พี่มุกกลับมาเเล้วค่า!!!!! เป็นยังไงกันบ้างคะปิดเทอมกันรึยังเอ่ย ปิดเทอมเเล้วน้องๆ เเต่ละคนมีเเผนทำอะไรกันบ้างคะ? ปิดเทอมเเบบนี้พี่มุกอยากเเนะนำให้น้องๆ ลองหากิจกรรมที่ชอบหรือสนใจอย่างเช่น เข้าค่ายอาสาหรือเล่นกีฬาดูนะคะเป็นการพักผ่อนจากการเรียนเเละเป็นการเรียนรู้ว่าตัวชอบอะไร อยากทำอะไร เพื่อใช้เป็นเเนวทางในการตัดสินใจเข้ามหาลัยได้อีกด้วย ครั้งหน้าพี่มุกจะมาเเนะนำกิจกรรมช่วงปิดเทอมที่น่าสนใจสำหรับน้องๆ กันส่วนวันนี้พี่มุกมีสรุป
สูตรเคมีเรื่องเเก๊สให้น้องๆ ไว้ใช้เตรียมตัวก่อนเปิดเรียนกันค่ะ พร้อมกันรึยังคะถ้าพร้อมเเล้วไปดูสรุปสูตรกันเลย ^^
ก่อนจะเริ่มสูตรพี่มุกอยากให้น้องๆ เข้าใจเนื้อหาเเละที่มาที่ไปของสูตรกันก่อนเพราะพี่มุกเชื่อว่าน้องๆ หลายคนคงเคยเป็นรวมถึงพี่มุกด้วยที่ตอนเรียนหรือตอนสอบจำสูตรได้นะท่องสูตรไปอย่างดีเลยจ้าเเต่ทำข้อสอบไม่ได้หรือทำได้ใส่สูตรคิดออกมีคำตอบในตัวเลือกเเต่เป็นคำตอบที่ผิดอ่ะ พี่มุกเลยกลับมาตั้งคำถามกับตัวเองว่าเป็นเพราะอะไรสุดท้ายได้คำตอบว่าเพราะไม่เข้าใจว่าทำไมต้องใช้สูตรนี้ , สูตรนี้มาจากไหน, ใช้เมื่อไหร่, ตัวเเปรเเต่ละตัวมีความหมายยังไงรวมๆคือไม่ได้เข้าใจเนื้อหาเเละมองภาพออกนั้นเอง (การเรียนที่ดีหรือการที่จะทำข้อสอบได้พี่มุกเชื่อว่าถ้าเรามองให้เป็นภาพทุกอย่างจะง่ายขึ้นทันทีซึ่งพี่มุกจะมาขยายเรื่องนี้ในบทความหน้านะคะ 🙂
กลับมาเข้าเรื่องกันจ้าเกริ่นมาซะยาวน้องๆ คงจะเคยได้ยินคำว่า ของเเข็งของเหลวเเก๊สกันมาบ้างเเล้วมันคืออะ? ทำไมต้องเรียนเรื่องนี้ในเคมี? พี่มุกจะพาน้องๆ มาหาคำตอบกัน
ของเเข็งของเหลวเเก๊ส คือ สถานะของสสาร (Phase of matter) โดยสสารจะเปลี่ยนสถานะเมื่อพลังงานเพิ่มขึ้นซึ่งสถานะหรือเฟสของสสารมีทั้งหมด 4 เเบบ ได้เเก่ ของเเข็ง, ของเหลว, เเก๊สเเละพลาสมา(พลาสมาน้องๆ จะได้เรียนในระดับมหาลัย)
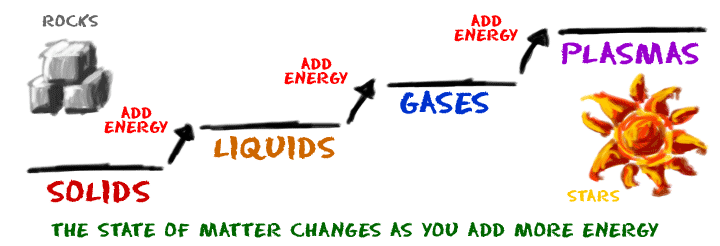
ขอบคุณรูปภาพจาก chem4kids
การเปลี่ยนเเปลงของสสารเกิดได้ 2 เเบบคือ
- การเปลี่ยนเเปลงทางฟิสิกส์ (ลักษณะภายนอกเปลี่ยน มองเห็นได้ )
- การเปลี่ยนเเปลงทางเคมี (เกิดการเปลี่ยนเเปลงภายในอะตอม ไม่สามารถมองเห็นได้ )
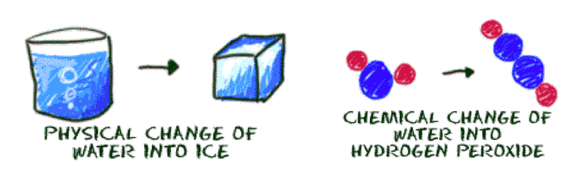
ขอบคุณรูปภาพจาก acamrmicheal
ถึงตรงนี้น้องๆ อาจรู้กันอยู่เเล้วว่าการเปลี่ยนสถานะเกิดเมื่ออุณหภูมิเปลี่ยน
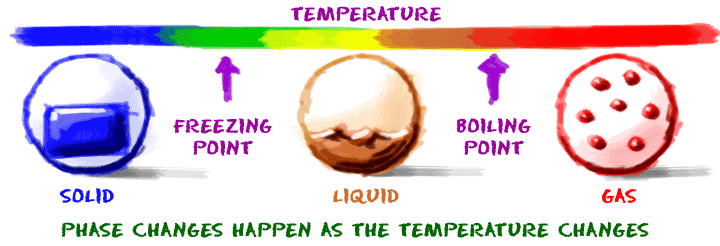
ขอบคุณรูปภาพจาก chem4kids
จากทั้ง 4 สถานะในรูปวันนี้พี่มุกจะพามาโฟกัสที่สถานะเเก๊สซึ่งบอกเลยว่าง่ายมากเพราะเป็นสิ่งที่น้องๆ สามารถโยงกับเรื่องในชีวิตประจำวันได้
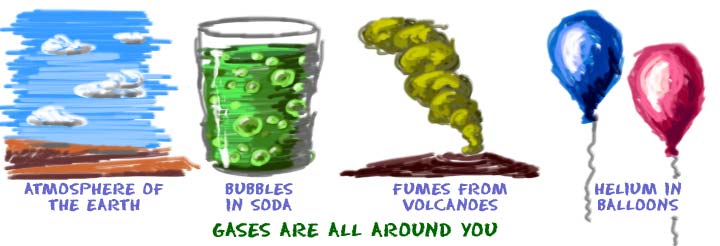
ขอบคุณรูปภาพจาก Ms. Johnson’s Chemistry
เห็นไหมคะว่ามีเเก๊สลอยไปลอยมาอยู่รอบๆ ตัวเราเสอมเเต่เราไม่สามารถสัมผัสได้เเต่ถ้าเราต้องการสัมผัสเเก๊สล่ะเราจะทำยังไงเเน่นอนว่าเราสัมผัสเเก๊สโดยตรงไม่ได้เเต่จับเเก๊สมาอยู่ในปริมาตรต่างๆ ได้เกริ่นมาถึงตรงนี้พี่มุกอยากให้น้องๆ ลองคิดดูว่ามีปัจจัยไหนบ้างที่มีผลต่อสถานะของเเก๊สลองคิดดูเเล้วมาดูเฉลยไปพร้อมๆกัน
คำตอบคือ อุณหภูมิ, ความดันเเละปริมาตรมาลองดูว่าเเต่ละปัจจัยส่งผลยังไง
- อุณหภูมิ : สำคัญมากเพราะมีผลต่อการเปลี่ยนสถานะ
- ความดัน : เป็นผลมาจากการเปลี่ยนเเปลงอุณหภูมิทำให้ความดันเปลี่ย
(อุณหภูมิสูงขึ้น –> ความดันเพิ่มขึ้น) - ปริมาตร : ใช้ระบุขอบเขตของเเก๊สที่ทำการศึกษาโดยปริมาตรขึ้นอยู่กับอุณหภูมิเเละความดัน
ต่อมาได้มีนักวิทยาศาสตร์ 3 คนอธิบายเรื่องเเก๊สจากความสัมพันธ์ของตัวเเปรต่างๆ ดังนี้
Gay-Lussac’s law : กฎของเกย์-ลูซเเซก
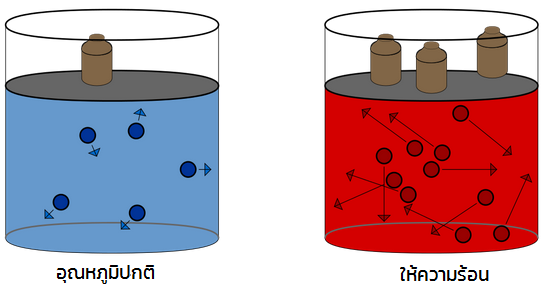
ขอบคุณรูปภาพจาก diverswhowanttolearnmore
การทดลองของเกย์-ลูซเเซกคือหาความสัมพันธ์ระหว่างอุณหภูมิกับความดันซึ่งถ้าให้เปรียบเทียบให้เห็นภาพคือในห้องมีซอมบี้อยู่ในอุณหภูมิปกติอยู่กันอย่างอิสระ(อนุภาคลอยอย่างอิสระ)เเล้วเมื่อเราเพิ่มอุณหภูมิในห้องให้สูงขึ้นซอมบี้ก็จะวิ่งกระจัดกระจายเร็วขึ้นด้วยเเรงที่มากขึ้น (อนุภาคเเก๊สเคลื่อนที่เร็วขึ้นเเรงดันภายในมากขึ้น) เพื่อดันประตูหาทางออกเราที่อยู่ข้างนอกถ้าจะขังให้ซอมบี้อยู่เเต่ในห้อง (ปริมาตรคงที่, มวลคงที่) ก็ต้องหาอะไรที่หนักขึ้นมาดันประตูไว้ (เพิ่มความดัน) เห็นไหมว่าง่ายนิดเดียวเเทบไม่ต้องจำสูตรเลยเเค่นึกภาพให้ออก
หลังจากเกย์ – ลูซเเซกทำการทดลองซ้ำๆ เเละนำผลที่ได้มาคำนวณจึงเกิดสูตรคือ
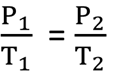
Boyle’s law : กฎของบอยล์
การทดลองของบอยล์คือเพิ่มความดันให้ระบบส่งผลให้ปริมาตรลดลงเเต่อุณหภูมิคงที่ สูตรคือ P1V1 = P2V2
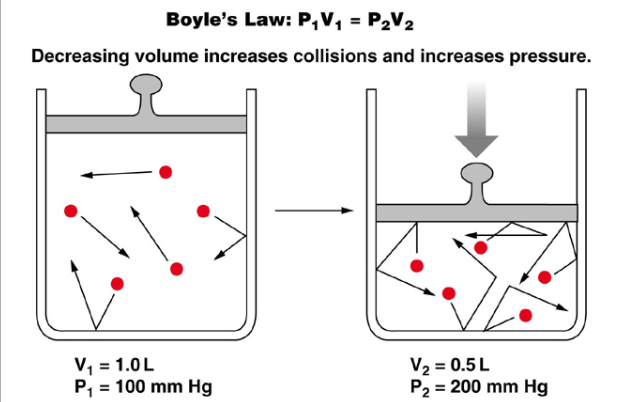
ขอบคุณรูปภาพจาก socratic
ตัวอย่างกฎของบอยล์ที่เห็นภาพได้ง่ายที่สุดคือการหายใจคือเมื่อน้องๆ หายใจเข้ากะบังลมและกล้ามเนื้อซี่โครงจะหดตัวเพิ่มขนาดของช่องอกและทำให้ปริมาตรปอดของใหญ่ขึ้น(ต้องการพื้นที่เพื่อเก็บอากาศให้ได้มากขึ้น)ความดันลดลงเพื่อให้อากาศไหลเข้าสู่ปอด ตรงข้ามกับการหายใจออกกล้ามเนื้อซี่โครงจะคลายตัวปริมาตรปอดลดลงทำให้เกิดแรงดันเพิ่มขึ้นและอากาศไหลออกจากปอด
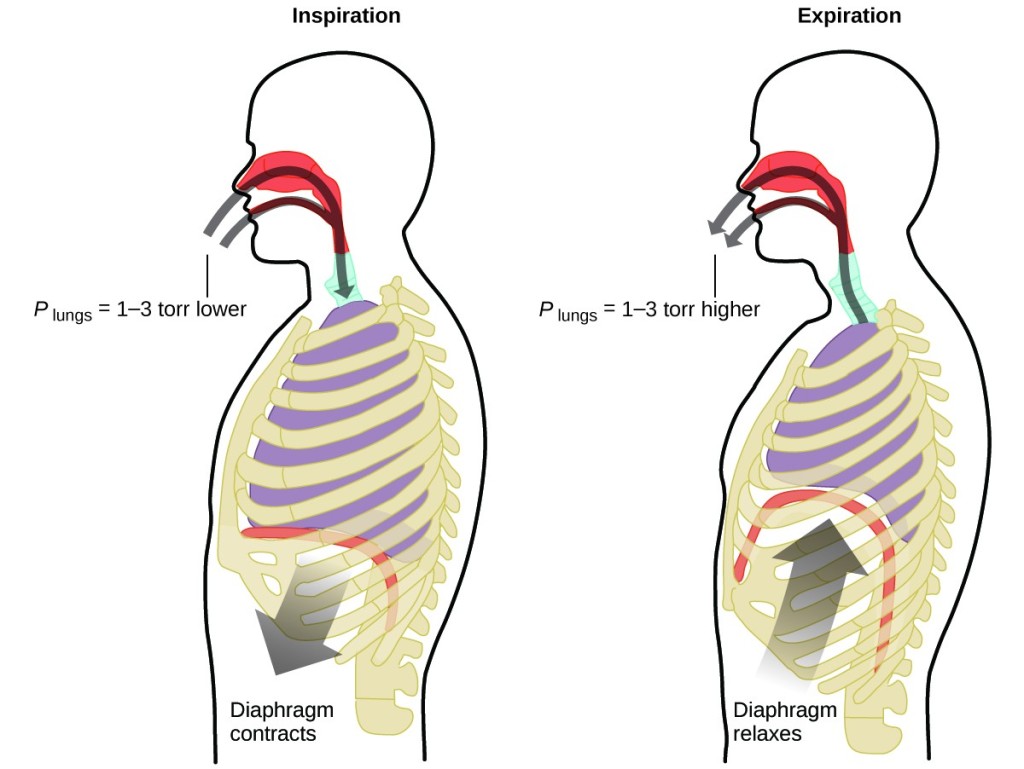
ขอบคุณรูปภาพจาก General College Chemistry I
Charles’s Law : กฎของชาร์ล
ชาร์ลทำการทดลองหาความสัมพันธ์ระหว่างอุณหภูมิกับปริมาตรคือเมื่อเพิ่มอุณหภูมิจะพบว่าปริมาตรจะเพิ่มขึ้นเมื่ออนุภาคได้รับความร้อนจะทำให้ปริมาตรเพิ่มขึ้นเเต่ความดันคงที่ สูตรกฎของชาร์ล
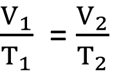
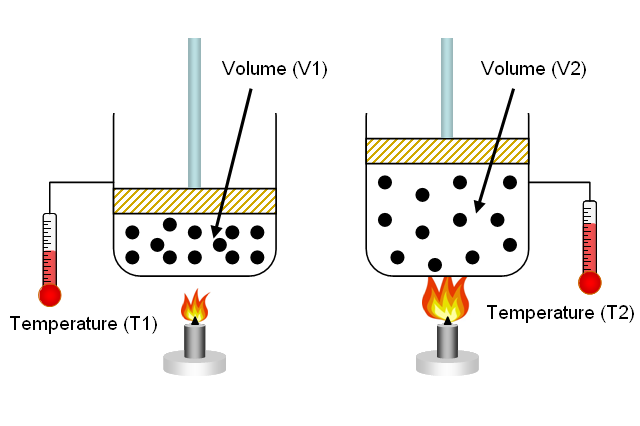
ขอบคุณรูปจาก astrocamp
จากทฎษฎีของทั้ง 3 คนเมื่อนำมารวมกันโดยให้ m คงที่จะได้สูตรที่เรียกว่ากฎรวมเเก๊ส
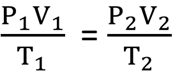
สุดท้ายเพื่อไม่ให้เกิดความยุ่งยากในการทำความเข้าใจนักวิทยาศาสตร์จึงคิด Ideal gas law (กฎเเก๊สในอุดมคติ) ซึ่งพี่มุกเชื่อว่าน้องๆ หลายคนคงเคยเห็นหรือรู้จักสูตรนี้กันมาบ้างเเล้ว
PV = nRT
R คิอค่าคงที่ = 0.082
ซึ่งจากสูตร Ideal gas law นี้สามารถเชื่อมโยงไปถึงกฎเเก๊สของทั้ง 3 คนที่ผ่านมาได้ดังนี้
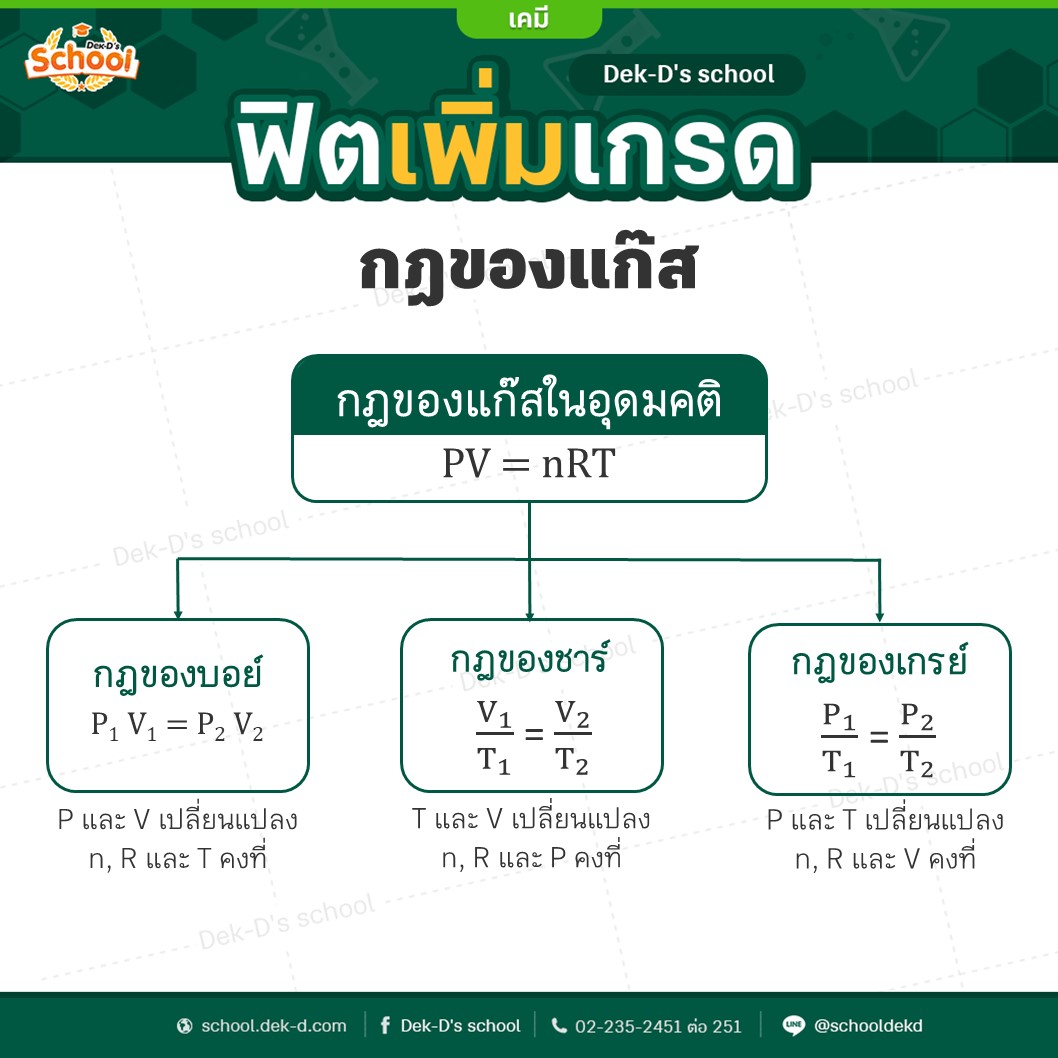
เห็นไหมคะว่าไม่ยากเลยถ้าน้องๆ มองทุกอย่างให้เป็นภาพเเละเชื่อมโยงกันทุกเรื่องที่เราเรียนหรือสนใจนั้นสามารถนำมาทำให้มองเห็นภาพได้ง่ายในชีวิตประจำวันค่ะ ^^
ส่วนน้องๆ คนไหนที่อยากเตรียมความพร้อมก่อนเปิดเทอมสามารถทดลองเรียนเเละดูรายละเอียดการสมัครเรียนได้ที่ เก่งเคมีม.ปลาย หรือ พิชิต TCAS เคมี: ปริมาณสารสัมพันธ์ ปฎิกิริยาเคมี สมดุลเคมี สอนโดยดร.โรจน์ฤทธิ์ โรจนธเนศ (อ.เต้) ผู้ช่วยศาสตราจารย์ประจำภาควิชาเคมี คณะวิทยาศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย โอกาสที่จะได้เรียนกับตัวจริงด้านเคมีแบบนี้มีไม่บ่อยห้ามพลาดนะคะเเละครั้งหน้าพี่มุกจะนำเทคนิคการเรียนเรื่องไหนมาเเชร์กันอย่าลืมติดตามหรือเข้ามาพูดคุยกันได้ที่ Facebook Dek-D School หรือ Line @schooldekd นะคะ 🙂



